Introduzione
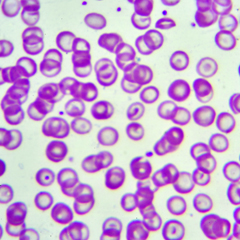
La talassemia è una malattia ereditaria del sangue che caratterizzata da una ridotta o assente produzione di emoglobina, la proteina contenuta nei globuli rossi con il compito di trasportare l'ossigeno in ogni parte del corpo.
La talassemia colpisce soprattutto le popolazioni dell’area mediterranea, dell'Asia meridionale, del sud-est asiatico e del Medio Oriente.
In Italia si stima siano circa tre milioni di portatori sani e circa 7000 le persone con la forma grave della malattia, concentrati prevalentemente in Sardegna, in Sicilia, nelle regioni meridionali ma anche nel delta padano e Veneto.
La talassemia si classifica in due tipologie principali: alfa e beta talassemia. In Italia e nell’area mediterranea la forma più diffusa è la beta-talassemia.
La forma più grave della malattia è rappresentata dalla beta-talassemia di tipo major, conosciuta anche come anemia mediterranea o morbo di Cooley. Altri tipi sono la beta-talassemia intermedia, l'alfa-talassemia major o idrope fetale, e la malattia da emoglobina H.
Con le parole talassemia minor, o microcitemia o tratto talassemico, si indica la condizione dei portatori sani, che non presentano particolari problemi di salute. Tuttavia, se entrambi i partner sono portatori sani (microcitemici) di beta-talassemia, il rischio genetico di generare figli con la forma grave di malattia è significativo a ogni gravidanza; pertanto, è fondamentale una consulenza genetica prima del concepimento o nelle prime settimane di gravidanza.
Esenzione, associazioni, centri
In Italia la talassemia è inserita nell'elenco delle malattie rare esenti dal costo del ticket (Decreto del Presidente del Consiglio dei Ministri del 12 gennaio 2017, Allegato 7) con il codice RDG010, che fa riferimento al più ampio gruppo delle Anemie ereditarie.
Per altre informazioni (centri di diagnosi e cura, associazioni di pazienti ecc.) sulle talassemie è possibile rivolgersi al Telefono Verde Malattie Rare (TVMR) 800.89.69.49, gratuito e attivo dal lunedì al venerdì dalle 9:00 alle 13:00. E’ possibile anche consultare il portale malattierare.gov.it
A livello europeo la talassemia è studiata all'interno delle ERN EuroBloodNet, la rete europea di centri esperti su patologie rare ematologiche. La missione dell’ERN è quella di ridurre e, alla fine, cancellare le disuguaglianze esistenti in Europa nell'ambito delle cure sanitarie rivolte ai pazienti con queste patologie, facilitando la condivisione delle conoscenze e agevolando la ricerca e l’erogazione dell’assistenza sanitaria a essa correlata.
Sintomi
La talassemia può causare una serie di problemi, per molti dei quali esistono trattamenti specifici.
Bambini e bambine con la forma più grave, la beta-talassemia major, di solito, manifestano i primi sintomi pochi mesi dopo la nascita.
Nelle forme meno gravi della malattia, invece, le prime manifestazioni potrebbero presentarsi durante l'infanzia o addirittura nell'età adulta. I portatori sani della malattia generalmente non hanno disturbi.
I principali problemi di salute legati alla malattia includono:
Anemia
Quasi tutte le persone con talassemia major o altre forme gravi sviluppano anemia che, nei casi più seri e senza adeguato trattamento può risultare fatale.
L'anemia comporta bassi livelli di emoglobina (proteina che trasporta l’ossigeno a tutto il corpo) nel sangue e si avvertono, generalmente, i seguenti disturbi:
- stanchezza, e una generale mancanza di energia (senso di affaticamento)
- mancanza di fiato
- battito cardiaco martellante e irregolare (palpitazioni)
- pallore del viso
- ingiallimento della pelle e degli occhi (ittero)
Nei casi più gravi la persona è costretta a periodiche e frequenti trasfusioni di sangue per tutta la vita.
Eccesso dei livelli di ferro
Nelle persone con talassemia major o altre forme gravi le ripetute trasfusioni di sangue determinano un aumentato rischio di sviluppare problematiche dovute ad un eccessivo accumulo di ferro nell'organismo. Ciò potrebbe causare:
- problemi di cuore,come l'alterazione e il manfunzionamento del muscolo cardiaco (cardiomiopatia), il battito cardiaco irregolare e l’insufficienza cardiaca
- ingrossamento del fegato e cirrosi epatica
- sviluppo sessuale (pubertà) ritardato
- bassi livelli di estrogeni (ormone femminile) o di testosterone (ormone maschile)
- diabete
- insufficiente funzionamento della ghiandola tiroidea (ipotiroidismo) e delle paratiroidi (ipoparatiroidismo)
Il trattamento standard per gestire e prevenire l'accumulo patologico di ferro (sovraccarico di ferro) nel corpo è la terapia chelante , o terapia di chelazione, cioè farmaci che si legano al ferro e lo eliminano dall’organismo.
Nelle forme gravi di talassemia possono presentarsi anche altri problemi, fra i quali:
- ritardo della crescita durante l'infanzia
- calcoli biliari (formazioni dure, simili a sassi, nella cistifellea) che possono causare l’infiammazione della colecisti (colecistite), mal di pancia (colica addominale) e colorazione gialla della pelle e delle muscose (ittero)
- crescita ossea inusuale, come un ingrossamento delle ossa del cranio (fronte, zigomi)
- ossa deboli, fragili (osteoporosi)
- ridotta fertilità, alcune persone affette da talassemia possono avere bisogno di cure specifiche
Cause
Le cause della talassemia sono genetiche ed ereditarie. Il tipo di talassemia che una persona ha dipende da quanti e quali tratti per la talassemia ha ereditato dai suoi genitori.
Nel caso in cui entrambi i genitori siano portatori sani di beta-talassemia c'è:
- 25% (1 su 4) di probabilità di generare un figlio con una talassemia grave (beta-talassemia major)
- 50% di probabilità di generare un figlio portatore sano (tipicamente asintomatico)
- 25% di probabilità di generare un figlio né malato né portatore
La talassemia alfa si trasmette ereditariamente in modo più complesso poiché interessa quattro geni potenzialmente difettosi, invece di due.
Figli di genitori portatori sani dell’alfa-talassemia potrebbero nascere con la malattia solo nel caso in cui ereditassero tre o quattro copie del gene difettoso; se, invece, ne ereditassero solo una o due copie sarebbero portatori sani.
Diagnosi
La malattia si diagnostica mediante uno specifico esame del sangue da eseguire, preferibilmente, presso un centro specializzato per questo tipo di analisi.
Il test può essere effettuato in qualsiasi momento della vita, dall'infanzia all'età adulta, per sapere se si è malati o portatori sani di beta-talassemia e, quindi, a rischio di avere un figlio con la forma grave della malattia.
Diagnosi prenatale
Nel corso della gravidanza una coppia "a rischio", con entrambi i partner portatori del gene mutato, può sottoporsi ad accertamenti durante la gravidanza mediante test molecolari per scoprire se il loro figlio nascerà con la talassemia. I principali test prenatali sono l'amniocentesi e la villocentesi.
Diagnosi post-natale
Nel neonato la malattia può essere diagnosticata tramite l'analisi del sangue fetale contenuto nel cordone ombelicale, oppure, attraverso un piccolo prelievo di sangue dal tallone del piede.
- test di primo livello, se sussiste una delle seguenti condizioni:
- avere un familiare portatore sano accertato
- avere una microcitosi (globuli rossi di volume inferiore alla norma) non dovuta a mancanza di ferro
- essere una coppia in età fertile che intende pianificare una gravidanza a prescindere dai parametri ematologici
- essere un adolescente o un adulto che vuole sapere se è o no portatore sano del tratto talassemico
- test di secondo livello, qualora nei risultati delle analisi di primo livello siano evidenziate alterazioni rispetto alla norma che facciano pensare ad una formadi talassemia grave o minore
Screening
Ad oggi, in Italia, non esiste un programma di screening neonatale obbligatorio e uniforme a livello nazionale per la ricerca della talassemia, ma in alcune regioni ad alta endemia (come Sardegna, Sicilia, Calabria, Puglia e zone del Ferrarese), esistono programmi regionali o iniziative locali che offrono screening gratuiti o consulenze genetiche specialmente per coppie in età fertile o in gravidanza al fine di individuare i portatori sani.
Terapia
Ad oggi il trattamento della beta-talassemia major o delle altre forme gravi comprende principalmente:
- trasfusioni di sangue
- rimozione del ferro in eccesso
- monitoraggio strumentale del ferro in eccesso
- trapianto di midollo osseo o di cellule staminali
- trattamento delle complicazioni della malattia
- rimozione della milza una volta posta la diagnosi di ipersplenismo (ovvero una milza iperattiva che distrugge i componenti del sangue come piastrine e globuli bianchi)
Recentemente, tuttavia, si stanno sperimentando anche nuove terapie avanzate, dalla terapia genica classica all’editing del genoma basato sulla CRISPR.
Trasfusioni di sangue
Per la maggior parte delle persone con talassemia major o altre forme gravi è necessario sottoporsi a regolari trasfusioni di sangue per curare l'anemia e a prevenire eventuali alterazioni delle ossa e dell'aspetto del volto, fegato e milza ingrossati e un aumento del volume del cuore.
Di solito, le trasfusioni si fanno in ospedale e richiedono poche ore ogni volta, ma la frequenza con cui devono essere effettuate dipende dal tipo di talassemia nella forma più grave, ad esempio, può essere necessaria una trasfusione una volta al mese. Trasfusioni molto frequenti possono provocare accumulo di ferro nel corpo che deve essere eliminato con specifici farmaci.richiedere medicinali specifici per la sua eliminazione.
Eliminazione del ferro in eccesso
La rimozione del ferro in eccesso dovuto alle trasfusioni di sangue è nota come terapia chelante o terapia di chelazione e va iniziata dopo circa 10 trasfusioni. Questo trattamento è molto importante perché livelli troppo alti di ferro nel corpo possono danneggiare gli organi.
I medicinali usati nella terapia di chelazione sono conosciuti come agenti chelanti. I principali ad oggi disponibili sono:
- desferoxamina (DFO), la somministrazione del farmaco avviene sottocute con infusione molto lenta (12 ore) e va ripetuta cinque o sei volte a settimana
- deferiprone (DFP), può essere preso in compresse o in forma liquida, tre volte al giorno; talvolta, è utilizzato insieme al DFO per ridurre il numero di infusioni
- deferasirox (DFX), compresse solubili da prendere una volta al giorno
Ogni farmaco ha i suoi vantaggi e svantaggi, pertanto è fondamentale che sia il medico a valutare e consigliare il medicinale migliore alla persona, caso per caso.
Monitoraggio strumentale del ferro in eccesso
Esistono diverse analisi per misurare in modo affidabile la quantità di ferro nell’organismo:
- LIC, test che misura la concentrazione del ferro nel fegato. Si esegue mediante biopsia epatica (prelievo di una piccolissima quantità di tessuto del fegato) e per questo richiede il consenso delle persone con talassemia e/o dei loro genitori
- SQUID, metodica non invasiva che si basa sulle proprietà paramagnetiche del ferro per misurarne la concentrazione nell'organismo. È una tecnica molto costosa, impegnativa dal punto di vista tecnologico, pertanto è disponibile solo in alcuni centri in Italia
- RMN, risonanza magnetica nucleare per immagin. È un metodo non invasivo e più facilmente disponibile sul territorio nazionale, rispetto alla SQUID. Le concentrazioni di ferro nel fegato ottenute con questo metodo sono molto affidabili. La RMN si è dimostrata uno strumento utile anche per la valutazione del sovraccarico di ferro nel cuore
Il trapianto di midollo osseo o di cellule staminali
Il trapianto del midollo osseo (TMO) rappresenta la cura definitiva per le persone con talassemia major. Le cellule staminali sono prodotte nel midollo osseo (il tessuto spugnoso che si trova all’interno delle ossa) e hanno la capacità di trasformarsi in diversi tipi di cellule del sangue.
La procedura consiste nella somministrazione alla persona con talassemia, attraverso una cannula collegata ad un ago posizionato in vena (fleboclisi) di cellule staminali, prelevate dal midollo osseo di un donatore sano compatibile. Le cellule staminali trasfuse sostituiscono quelle difettose difettose e iniziano a produrre globuli rossi sani che vanno a sostituire quelli difettosi nel corpo del ricevente. Questa terapia è limitata dalla disponibilità di un donatore compatibile e da una serie di altri fattori come, ad esempio, lo stato complessivo di salute del malato e l'assenza di danni gravi al fegato.
Le cellule staminali sono prodotte nel midollo osseo (il tessuto spugnoso che si trova nelle ossa) e hanno la capacità di trasformarsi in diversi tipi di cellule del sangue.
Nel trapianto di cellule staminali, le cellule di un donatore sano sono trasferite al malato attraverso una cannula collegata ad un ago posizionato in una vena (fleboclisi). Quando arrivano nel corpo del malato, le cellule staminali trasfuse iniziano a produrre globuli rossi sani che vanno a sostituire quelli difettosi.
Sebbene questa procedura possa essere effettuata con successo, è una cura intensiva che comporta una serie di rischi anche gravi. Prima di programmare il TMO devono essere attentamente valutati i rischi e i benefici caso per caso. I risultati migliori si otttengono se il midollo osseo proviene da un fratello o da una sorella che sia completamente istocompatibile.
Le complicanze includono, infezione e sanguinamento, che si verificano solitamente prima che il midollo del donatore abbia sostituito il midollo del ricevente; il rigetto delle cellule trapiantate da parte del sistema immunitario del ricevente; la malattia da trapianto contro lʼospite (GvHD), per cui il midollo del donatore riconosce il paziente ricevente come “estraneo” e provoca alterazioni della pelle, dell’intestino e del fegato che possono essere lievi, gravi o fatali.
Una valida alternativa al TMO oggi è il trapianto da cordone ombelicale (CO) come fonte di cellule staminali emopoietiche. Questa metodica, utilizzata prevalentemente in età pediatrica e in pazienti di basso peso corporeo (generalmente sotto i 40-50 kg), offre molti vantaggi rispetto al trapianto tradizionale, specialmente in assenza di un donatore familiare perfettamente compatibile.
Il trattamento delle complicazioni della malattia
La talassemia può causare una serie di problemi che potrebbero dover essere gestiti con:
- terapia ormonale, utile nei casi di pubertà (maturazione sessuale) ritardata e per la cura di bassi livelli ormonali
- vaccinazioni e antibiotici, per prevenire e curare le infezioni
- ormoni tiroidei, in caso di problemi con la ghiandola tiroide (ipotiroidismo)
- bifosfonati, farmaci per aiutare a rafforzare le ossa nei casi di fragilità (osteoporosi)
- intervento chirurgico di rimozione della cistifellea per eliminare i calcoli biliari
Bambini e adulti con forme gravi di talassemia dovrebbero essere supportati da un team multidisciplinare di diversi sanitari.
Nuove strategie terapeutiche
Nell’ultimo decennio si sono ottenuti notevoli risultati nella sperimentazione di terapie avanzate alternative al trapianto di midollo che hanno come prospettiva la guarigione e l’indipendenza dalle trasfusioni di sangue: la terapia genica e l’editing genomico.
La terapia genica
La terapia genica classica si basa sull’introduzione nelle cellule staminali ematopoietiche delle persone con beta-talassemia di un gene beta-globinico “sano” (un gene che fornisce le istruzioni per produrre la beta-globina, una delle subunità dell’emoglobina) per correggere gli effetti di quello “malato”. Il trasferimento di materiale genetico tramite vettori lentivirali di nuova generazione, che rappresenta una delle tecnologie più avanzate e sicure nel campo della terapia genica. Si tratta di virus ingegnerizzati per agire come "navette" in grado di trasportare geni terapeutici all'interno delle cellule, senza tuttavia causare malattie. Con questa tecnica si è raggiunto un risultato molto promettente: circa il 90% delle persone trattate è guarito e non ha più bisogno di trasfusioni.
L’editing genetico (CRISPR)
Altro approccio è quello basato sull’editing del genoma per riattivare la produzione di emoglobina fetale. La tecnica CRISPR, infatti, consente di effettuare la modifica direttamente sul DNA delle cellule staminali prelevate dal paziente. Questo approccio offre una possibilità di cura indipendente dalla disponibilità di un donatore ed elimina rischi di rigetto o di malattia da trapianto contro l’ospite. La tecnica prevede la raccolta delle cellule staminali del paziente (aferesi), la correzione in laboratorio ("cell factory") e la re-infusione dopo una chemioterapia mieloablativa (che serve a distruggere le cellule malate del midollo osseo per fare spazio alle cellule modificate in laboratorio). La durata del percorso terapeutico è di circa 6/8 mesi. Recenti studi hanno mostrato la completa indipendenza dalle trasfusioni nel 98% dei pazienti talassemici trattati, con risultati duraturi. La prima terapia genica basata sulla tecnologia CRISPR-Cas9 a ottenere la rimborsabilità in Italia è stata approvata il 17 settembre 2025, per trattare la beta-talassemia trasfusione-dipendente e l'anemia falciforme severa.
Prevenzione
La talassemia major conosciuta anche come anemia mediterranea o morbo di Cooley, è una malattia grave che dura per tutta la vita, per questo è importante fare prevenzione.
È importante identificare i giovani microcitemici fin dall'adolescenza o in età fertile e renderli consapevoli della loro condizione, in modo che conoscano i rischi di concepire un figlio con un partner microcitemico.
Accade spesso, infatti, che coppie di portatori sani di talassemia, non avendo disturbi, non sappiano di esserlo e quindi non conoscano i rischi legati ad una eventuale gravidanza. Un percorso di prevenzione e counseling genetico permetterà loro di affrontare con consapevolezza ogni strada scelta.
Vivere con
Molto si può fare per rimanere il più possibile in salute se si convive con la talassemia, oltre a seguire le terapie e sottoporsi ai necessari controlli.
Uno stile di vita sano
È importante:
- seguire una dieta sana e bilanciata. Normalmente non è necessaria una dieta speciale, sebbene a volte possa essere consigliato prendere degli integratori, come l'acido folico, il calcio o la vitamina D. Tuttavia, chi si sottopone regolarmente alle trasfusioni deve seguire una dieta a basso contenuto di ferro per evitarne l'accumulo. Sulle etichette degli alimenti è generalmente elencata la percentuale di ferro, leggerla con attenzione consente di evitare quelli con le quantità più elevate
- svolgere un'attività fisica regolare. Dopo aver ricevuto il parere positivo del medico curante, fare attività in cui il peso del corpo gravi sulle ossa (camminata, ballo, etc.) contribuisce a rafforzarle e a ridurre il rischio di osteoporosi
- evitare di fumare e di bere eccessive quantità di alcolici. Ciò aiuta a mantenere sani ossa e cuore
- proteggersi dalle infezioni. Lavarsi le mani con acqua e sapone regolarmente, evitare il contatto ravvicinato con persone malate, quando possibile, e assicurarsi di aver effettuato tutte le vaccinazioni
Gravidanza e contraccezione
Le donne con la talassemia major o altre gravi forme possono portare a termine una gravidanza partorendo un figlio sano ma è importante che consultino prima il medico curante o il ginecologo:
- perché il partner potrebbe essere un portatore sano di talassemia. In tal caso è necessaria una consulenza genetica per discutere delle possibili conseguenze
- per valutare l'eventuale necessità di assumere farmaci per la fertilità
- per considerare gli eventuali rischi che possano presentarsi durante la gravidanza, ad esempio problemi di cuore nella madre e di crescita nel bambino
- per valutare con un attento mnitoraggio della gravidanza l'eventuale necessità di modifica delle terapie in atto
Se non si sta programmando una gravidanza, è consigliabile utilizzare una forma affidabile di contraccezione.
Precauzioni in caso di interventi chirurgici
Nel caso si debba affrontare un intervento chirurgico in anestesia generale è importante informare il chirurgo e i medici curanti della propria condizione di talassemici. L'anestesia generale, infatti, può causare problemi come l'aumento della probabilità di eventi trombotici. Per ridurre il rischio di complicazioni, potrebbe essere necessario un attento monitoraggio durante l'intervento e una trasfusione di sangue prima o dopo.
Quando consultare il medico
La talassemia può causare una serie di problemi gravi che possono insorgere anche in maniera improvvisa e richiedere l'intervento di un medico o il ricovero in ospedale.
Si deve fare particolare attenzione a:
- temperatura elevata (febbre) da 38°C in su
- brividi
- diarrea e vomito
- battito cardiaco veloce
- respirazione rapida
- vertigini o svenimenti
- improvviso dolore o gonfiore della addominale
- peggioramento dell'ingiallimento della pelle o degli occhi (ittero)
- debolezza degli arti
- battito cardiaco martellante e irregolare (palpitazioni)
- sonnolenza
- convulsioni (crisi convulsive)
Se si verifica uno qualsiasi di questi segnali contattare immediatamente il medico curante. Se non è possibile, è consigliabile recarsi al più vicino pronto soccorso o chiamare un'ambulanza. È necessario avvertire il personale medico che si è talassemici.
Essere portatore sano di talassemia
Un portatore sano è una persona che ha un solo gene difettoso per la sintesi dell'emoglobina e, quindi, alterazioni minime che non provocano sintomi evidenti. Questa situazione è definita anche talassemia minor. Spesso, il portatore sano non sa di esserlo perché non ha segnali di malattia e viene a conoscenza della propria condizione a seguito di un semplice esame del sangue presso un centro specializzato. In queste persone i globuli rossi sono in numero maggiore rispetto al normale ma sono un po’ più piccoli (da cui il nome di microcitemia) e più poveri di emoglobina. Il gene sano, comunque, consente una produzione di globuli rossi e di emoglobina più che sufficiente per condurre una vita normale.
Analisi per scoprire di essere portatori sani
Chiunque può chiedere di sottoporsi ad un'analisi per scoprire se sia portatore sano di talassemia in qualsiasi momento della vita. Può essere particolarmente utile se:
- nella propria famiglia sono presenti persone malate di talassemia (storia familiare di talassemia)
- si è sessualmente attivi e si vuole scoprire se si sia a rischio di generare un figlio con talassemia
- si è a conoscenza che il proprio partner è portatore/ice sana e si vuole verificare di non essere nella stessa condizione perché ciò aumenterebbe il rischio di generare figli malati
Avere dei figli
I portatori sani, sono a rischio di procreare figli talassemici solo nel caso in cui anche il partner sia un portatore sano o abbia la talassemia.
Se si ha intenzione di avere un figlio, quindi, è raccomandabile che il proprio partner si sottoponga alle analisi per verificare di non essere anche lui o lei un portatore sano.
Nel caso in cui entrambi i genitori siano portatori sani del tratto beta-talassemico (forma beta della talassemia ) per ogni gravidanza vi è:
- 25% di probabilità (1 su 4) che il bambino non erediti i geni difettosi e non abbia la talassemia, né possa trasmetterla
- 50% di probabilità (1 su 2) che il bambino erediti solo una copia del gene difettoso da uno dei genitori e sia quindi portatore sano
- 25% di probabilità (1 su 4) che il bambino erediti le copie del gene difettoso da entrambi i genitori e nasca quindi con una talassemia grave (beta-talassemia major)
Se entrambi i partner sono portatori sani, prima di cercare una gravidanza è importante che ne informino il proprio medico e consultino un genetista che possa spiegare loro i rischi per i nascituri e le possibili azioni da intraprendere.
Possibili problemi di salute
Il portatore sano di talassemia non svilupperà mai la talassemia grave. Potrà vivere una vita normale, senza problemi significativi per la salute.
Tuttavia, potrebbe avere una lieve anemia, con livelli bassi di emoglobina (la proteina che trasporta l'ossigeno a tutto l'organismo) nel sangue. Come conseguenza, potrebbe provare stanchezza e apparire di colorito pallido. L'anemia può essere riscontrata solo sottoponendosi a un'esame del sangue. In caso di risultato positivo, tuttavia, non si devono prendere di propria iniziativa integratori a base di ferro a meno che le analisi non rivelino che si tratti di una forma causata dalla sua mancanza (anemia sideropenica). Anche in questo caso dovrà essere il medico a prescrivere, se necessario, il trattamento più adeguato.
Portatori di altre malattie del sangue
I portatori di talassemia, per conoscere gli eventuali rischi di avere un figlio malato, dovrebbero fare una consulenza genetica anche nel caso in cui il loro partner fosse portatore di un tipo di disturbo diverso ma riguardante sempre un'anomalia dell'emoglobina:
- emoglobina C (HbC)
- emoglobina D (HbD)
- emoglobina E (HbE)
- emoglobina lepore
- anemia falciforme
Aspetti di genere
La beta-talassemia è una malattia genetica che colpisce nella stessa misura maschi e femmine. Tuttavia, esistono differenze significative di genere per quanto riguarda la gestione clinica, l’impatto della patologia e le complicanze:
- complicanze ormonali ed endocrinologiche: le donne con beta-talassemia trasfusione dipendente (TDT) grave spesso affrontano delle sfide specifiche legate allo sviluppo puberale con cicli mestruali irregolari o addirittura assenti (amenorrea) che possono richiedere anche terapie ormonali sostitutive. Queste complicanze sono spesso la conseguenza del sovraccarico di ferro che colpisce le ghiandole endocrine provocando seri danni
- gravidanza e fertilità: la gestione della fertilità è quasi esclusivamente femminile e richiede un monitoraggio continuo per la gestione del rischio di complicazioni cardiache e per l’adattamento della terapia chelante e dei livelli di ferro prima e durante la gravidanza
- osteoporosi: sebbene sia comune in entrambi i generi, le donne con beta-talassemia presentano un’insorgenza di demineralizzazione ossea più precoce o più grave, probabilmente influenzata anche da squilibri ormonali legati all’ipogonadismo
- gestione del sovraccarico di ferro: persone con beta-talassemia TDT accumulano ferro in eccesso a causa delle frequenti trasfusioni, anche ogni 2-3 settimane. Recenti studi evidenziano un rischio significativamente più alto nei maschi di sviluppare complicanze cardiache quali disfunzione cardiaca, scompenso ed aritmie, sebbene il sovraccarico di ferro sia comparabile in entrambi i sessi. L’ipotesi è che le donne con talassemia abbiano una migliore tolleranza allo stress ossidativo indotto dall’accumulo di ferro cardiaco con conseguente bisogno di una terapia chelante del ferro personalizzata
- impatto psicologico e qualità della vita: la necessità di trasfusioni regolari ogni 2-3 settimane condiziona in generale molto la qualità della vita, tuttavia, studi di medicina di genere evidenziano un carico emotivo maggiore nelle donne legato alla gestione quotidiana delle cure e alle limitazioni nella vita professionale e sociale
Bibliografia
Liang D, Schmidt-Wolf IGH, Pu J. New Gene Therapy Strategy for β-Thalassemia [Sintesi]. Stem cell reviews and report. 2026
Cheng AN, Kwiatkowski JL. Current therapeutic landscape of β-thalassemia: focus on gene therapy. Therapeutic advances in rare disease. 2026; 7
Levesque S, Bauer DE. CRISPR-based therapeutic genome editing for inherited blood disorders [Sintesi]. National revew of drug discovery. 2025; 24(12): 907-925
Ballantine J, Tisdale JF. Gene therapy for sickle cell disease: recent advances, clinical trials and future directions [Sintesi]. Cytotherapy. 2025; 27(7): 826-834
Laurent M, Geoffroy M, Pavani G, Guiraud S. CRISPR-Based Gene Therapies: From Preclinical to Clinical Treatments [Sintesi]. Cells. 2024; 13(10): 800
Fianza PI, Rahmawati A, Wijaya I, et al. Gender Disparities in Psychological Disturbances and Quality of Life Among Adolescent and Adult Patients with Thalassemia: A Review. Journal of multidisciplinary healthcare. 2024; 17: 1663-1669
Makis A, Voskaridou E, Papassotiriou I, Hatzimichael E. Novel Therapeutic Advances in β-Thalassemia. Biology (Basel). 2021; 10(6): 546
Magrin E, Miccio A, Cavazzana M. Lentiviral and genome-editing strategies for the treatment of β-hemoglobinopathies. Blood. 2019; 134(15): 1203-1213
Pepe A, Gamberini MR, et al. Gender differences in the development of cardiac complicationa: a multicenter study in a large cohort of thalassaemia major patients to optimize the timing of cardiac follow-up [Sintesi]. The British Journal of Hematology. 2018; 180: 879-888
Ivaldi G, Barberio G. Raccomandazioni per la diagnostica di primo livello delle emoglobinopatie della Società Italiana Talassemie ed Emoglobinopatie-SITE. Collana Scientifica S.I.T.E. 2012, 1
Ministero della Salute, Istituto Superiore di Sanità (ISS), Centro per la valutazione dell'efficacia dell'assistenza sanitaria (CeVEAS). Linea Guida 20: Gravidanza Fisiologica. 2011
Ryan K, Bain BJ, Worthington D, James J, Plews D, Mason A. et al. Significant haemoglobinopathies: guidelines for screening and diagnosis. British Journal of Haematology. 2010; 149: 35-49
Cao A, Galanello R. Beta-thalassemia. Genetics in Medicine. 2010; 12(2): 61-76
Prossimo aggiornamento: 07 Maggio 2028




























