Introduzione
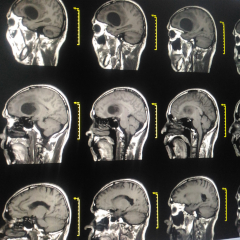
Il glioblastoma, noto anche come glioblastoma multiforme o astrocitoma di grado IV, è una forma molto aggressiva di tumore che colpisce il sistema nervoso centrale. Sebbene si manifesti quasi esclusivamente nel cervello, il glioblastoma può anche apparire nel tronco cerebrale, nel cervelletto e nel midollo spinale. Rappresenta circa il 45% di tutti i tumori che hanno origine nel cervello. Il glioblastoma ha origine da un gruppo di cellule, chiamato glia, che svolge una funzione di sostegno per le cellule nervose, i neuroni.
Incidenza e sopravvivenza
Il glioblastoma insorge più frequentemente in età matura tra i 45 e i 75 anni, ma può presentarsi a qualsiasi età, inclusa l'infanzia. La frequenza di nuovi casi (incidenza) è stimata intorno a 3-4 casi su 100 mila abitanti per anno con un tasso leggermente superiore negli uomini rispetto alle donne (1.6:1) e nelle persone di origine caucasica.
La sopravvivenza mediana è di circa 15 mesi con un tasso di sopravvivenza di circa il 5% a 5 anni dalla diagnosi dopo trattamento con radioterapia e chemioterapia con temozolomide.
I glioblastomi possono essere classificati come primari, o de novo, vale a dire come neoplasie aggressive e altamente invasive non derivanti da altre malattie. Di solito, infatti, non si accompagnano a evidenze cliniche, radiologiche o istopatologiche di precedenti malattie o precedenti lesioni (gliomi di basso grado). Meno comunemente, i glioblastomi possono presentarsi come secondari, vale a dire derivanti dalla progressione degli astrocitomi di basso grado.
La cura di questo tumore è molto difficile, anche se con la terapia è possibile rallentarne la progressione e ridurne i disturbi (sintomi).
Sintomi
Il glioblastoma è un tipo di tumore del cervello altamente maligno che si manifesta con mal di testa di crescente intensità, nausea, vomito e attacchi epilettici. Tali disturbi sono causati dalla massa tumorale che, espandendosi all'interno del cranio, provoca un aumento di pressione e la dilatazione dei vasi sanguigni cerebrali. I disturbi (sintomi) possono essere anche di tipo neurologico e non specifici, come disturbi della personalità o dello stato di coscienza.
Cause
Originariamente, si pensava che i glioblastomi derivassero esclusivamente da cellule gliali; tuttavia, numerose evidenze sperimentali suggeriscono che possano derivare da più tipi di cellule con proprietà simili a cellule staminali neurali (le cellule progenitrici da cui originano per differenziamento tutte le diverse cellule che compongono il sistema nervoso). Tutte queste cellule (cellule staminali, neuroni, glia) presentano numerose alterazioni molecolari che sono responsabili del loro comportamento anomalo. Invece di produrre tessuto normale, infatti, generano una massa tumorale creando una rete di vasi sanguigni che la alimenta.
Fattori di rischio
Le radiazioni ionizzanti sono uno dei pochi fattori associati ad un aumento del rischio di sviluppare un glioblastoma. Esempi di radiazioni ionizzanti sono i raggi X, utilizzati nelle radiografie e nella TAC, i raggi gamma, usati nella PET o nelle scintigrafie, oltre ai raggi ultravioletti, compresa la quota emessa dal sole. Naturalmente gli effetti dipendono dal tipo di radiazione, dalla dose, dalla durata dell'esposizione e dalle zone del corpo esposte.
Casi di glioblastoma indotti dalle radiazioni sono stati osservati anni dopo l'esposizione a trattamenti con radioterapia, indicati per un altro tumore o altra condizione clinica. Altre esposizioni ambientali al cloruro di vinile, ai pesticidi, al fumo, alla raffinazione del petrolio e alla produzione di gomma sintetica sono state vagamente associate allo sviluppo dei gliomi. Al contrario, campi elettromagnetici, formaldeide e radiazioni non ionizzanti dai telefoni cellulari non hanno dimostrato di causare il glioblastoma.
Un aumento del rischio di sviluppo del glioblastoma si riscontra in alcune malattie genetiche specifiche, come la neurofibromatosi 1 e 2, la sclerosi tuberosa, la sindrome di Li-Fraumeni, il retinoblastoma e la sindrome di Turcot; tuttavia, meno dell'1% delle persone con un glioblastoma ha una malattia ereditaria nota.
Diagnosi
Le tecniche per accertare (diagnosticare) il glioblastoma sono:
- visita neurologica, volta ad individuare i disturbi (sintomi) attraverso il controllo della vista, dell'udito, dello stato di equilibrio e della capacità di coordinare i movimenti, della forza fisica e dei riflessi. Eventuali problemi rilevati attraverso tali controlli offrono indizi per scoprire l'area colpita dal tumore cerebrale
- esami strumentali per immagini, insieme di tecniche volte a individuare la sede e le dimensioni del tumore; in genere, si ricorre alla risonanza magnetica nucleare associata a speciali metodiche di imaging, quali la risonanza magnetica funzionale e la spettroscopia di risonanza magnetica. Altri strumenti di questo tipo includono la TAC (Tomografia assiale computerizzata) e la PET (Tomografia a emissione di positroni)
- biopsia (prelievo di un campione di tessuto da analizzare), effettuata tramite un ago, prima o durante l'intervento chirurgico di rimozione del glioblastoma, a seconda dei casi e in base alla posizione del tumore. Il frammento di tessuto viene analizzato in laboratorio per identificare la tipologia di cellule tumorali e il loro grado di aggressività. Test specifici rivelano anche le mutazioni genetiche presenti nelle cellule in esame e servono per fornire indizi sulla evoluzione della malattia e sulla terapia da effettuare
Terapia
Con la terapia è possibile rallentare la progressione della malattia e ridurne i sintomi.
La cura del glioblastoma richiede un approccio multidisciplinare. L'attuale terapia standard prevede la massima rimozione (resezione) chirurgica del tumore che possa essere effettuata in sicurezza, seguita da radiazioni con somministrazione concomitante di temozolomide, un agente chemioterapico detto alchilante orale. Successivamente, il protocollo prevede chemioterapia con temozolomide (Protocollo Stupp).
La rimozione chirurgica estesa e completa del glioblastoma è difficile perché questi tumori sono invasivi e spesso si localizzano in aree fondamentali del cervello, comprese le aree che controllano il linguaggio, la funzione motoria e i sensi. A causa dell'elevato grado di invasività, l'eliminazione della massa tumorale primaria non è curativa e le cellule tumorali infiltranti rimangono invariabilmente all'interno del cervello circostante, portando a una successiva progressione o ricomparsa della malattia.
Le terapie previste per il trattamento del glioblastoma sono:
- intervento chirurgico, il neurochirurgo interviene per rimuovere il tumore, operando in modo da eliminare tutte le parti di tessuto colpite e riducendo così la pressione che il tumore esercita all'interno del cranio, in modo da ridurre i disturbi (sintomi). Tuttavia, poiché le cellule del glioblastoma sono altamente infiltranti, esso riesce ad espandersi nel cervello diramandosi nelle diverse aree ed è impossibile procedere alla sua rimozione completa; per questo motivo, dopo l'intervento occorre sottoporsi a trattamenti mirati contro le cellule tumorali residue. Inoltre, con la neurochirurgia si possono prelevare frammenti di tessuto malato per effettuare un'analisi istologica del tumore al fine di impostare la terapia più adeguata
- radioterapia, tecnica che impiega radiazioni ad alta energia, come i raggi X, o fasci di protoni, per neutralizzare le cellule cancerose (Video). Durante le sedute di radioterapia si resta distesi mentre un'apposita apparecchiatura viene posizionata per proiettare i raggi sul punto specifico da trattare; la radioterapia si effettua, di solito, a seguito dell'intervento chirurgico e può essere associata alla chemioterapia (trattamento farmacologico); nei casi in cui non sia possibile procedere chirurgicamente, la terapia si baserà sin dall'inizio su applicazioni combinate di radioterapia e chemioterapia
- chemioterapia, consiste nella somministrazione di farmaci mirati ad annientare le cellule tumorali; in alcuni casi, nel corso dell'intervento chirurgico, si applicano alcune ostie (wafer) impregnate di farmaco che rilasciano la sostanza chemioterapica gradatamente fino a dissolversi (Video). La terapia per bocca, dopo l'intervento chirurgico, e durante o dopo la radioterapia, prevede l'assunzione di capsule di un farmaco, il cui principio attivo è il temozolomide. La chemioterapia per il glioblastoma spesso prevede la somministrazione del farmaco per via endovenosa
- terapia con i campi elettrici, è una tecnica mirata ad inibire la capacità di moltiplicarsi propria delle cellule tumorali e si basa sull'applicazione di tamponi adesivi sul cuoio capelluto, collegati a un dispositivo portatile che genera campi elettrici. Questa terapia si può abbinare alla chemioterapia e può essere praticata dopo l'intervento chirurgico
- terapia farmacologica mirata (terapia bersaglio), impiega farmaci che agiscono su specifiche anomalie delle cellule tumorali responsabili del loro accrescimento e della loro proliferazione. Tali sostanze inibiscono i processi di moltiplicazione cellulare annientando le cellule stesse. I farmaci a base di bevacizumab sviluppano un meccanismo d'azione che intercetta i segnali trasmessi dalle cellule del glioblastoma verso l'organismo, volti a incrementare la circolazione sanguigna e quindi il nutrimento delle cellule tumorali. Si tratta di un'opzione di cura farmacologica da adottare nel caso di inefficacia di altre cure
- sperimentazioni cliniche, sono studi per lo sviluppo di nuove possibilità di cura. Hanno il vantaggio di prospettare i trattamenti più avanzati, anche se non è sempre possibile determinare il rischio di effetti collaterali; di conseguenza, occorre sempre che sia il medico a valutare se una persona abbia o meno i requisiti per essere reclutato in una sperimentazione di nuovi farmaci. In seguito ai risultati incoraggianti di uno studio italiano di fase II (REGOMA), l’Agenzia Italiana del Farmaco (AIFA) il 19 dicembre 2019, ha inserito un nuovo farmaco, il regorafenib nell’elenco dei farmaci erogabili con procedura anticipata, cioè a carico del Servizio Sanitario Nazionale, che potrà essere prescritto ai pazienti colpiti da recidiva di un glioblastoma multiforme che non rispondono ad altre terapie. Il regorafenib è una molecola in grado di inibire le “strade” alternative che il tumore percorre per farsi largo nel tessuto sano e ostacola diversi meccanismi della crescita tumorale: dall’angiogenesi agli stimoli derivanti dal microambiente cellulare. Questo farmaco è riservato ai pazienti con recidiva in buone condizioni cliniche, che rappresentano circa il 30% di tutti i pazienti che hanno ricevuto una terapia di prima linea: in Italia, circa 1000 pazienti all’anno
- cure palliative, consistono in trattamenti medici volti ad attenuare il dolore o i disturbi (sintomi) legati a malattie gravi, senza però risolverne la causa. Il personale specializzato per questo tipo di cure assiste la persona che ne ha bisogno, i suoi familiari e lo staff dei medici curanti per offrire supporto supplementare alle cure in corso, in particolare dopo l'intervento chirurgico, durante le applicazioni di chemioterapia o radioterapia
Aspetti di genere
Il glioblastoma mostra differenze di genere rilevanti, sia come incidenza che come mortalità. È infatti più frequente negli uomini, con un rapporto uomini: donne di 1.6:1, e ha una sopravvivenza media dalla diagnosi di 15 mesi per gli uomini e 25.5 per le donne.
Per il sesso femminile sono stati riportati tumori di dimensioni maggiori associati a aree di necrosi più estese. Sono presenti anche differenze nella localizzazione preferenziale del tumore: più frequentemente nel lobo temporale sinistro negli uomini e nel lobo destro nelle donne.
Queste differenze sembrano almeno in parte dipendere dagli ormoni sessuali, in particolare dal principale ormone maschile, il testosterone, che interagendo con il suo recettore induce proliferazione cellulare.
Il ruolo degli ormoni femminili, estrogeni e progesterone, è meno chiaro, sebbene l’aumento del rischio di glioblastoma associato a menarca tardivo e menopausa precoce confermi il ruolo protettivo di questi ormoni, come è già dimostrato in altri tumori.
Poiché l’età media di insorgenza del glioblastoma è di 64 anni, quindi nel periodo post-menopausa, accanto agli estrogeni va considerato il coinvolgimento di altri fattori. Inoltre, la maggiore frequenza di glioblastoma nei maschi anche in età pediatrica, quando gli ormoni sessuali non hanno un ruolo rilevante, supporta una regolazione complessa.
Alla base delle differenze tra i sessi troviamo anche specificità genetiche, epigenetiche e del sistema immunitario. Differenze di espressione genica suggeriscono alla base del dimorfismo osservato nel glioblastoma il coinvolgimento di due importanti oncosoppressori, p53 e RB1 e più in particolare la loro inattivazione negli astrociti, le principali cellule del sistema nervoso centrale. Tale inattivazione è più evidente nelle cellule maschili di glioblastoma rispetto a quelle femminili. Parallelamente, i glioblastomi femminili esprimono livelli più alti di p21 e p27, entrambi fattori che inibiscono il ciclo cellulare. L’inattivazione contemporanea di p21, p27 e p16, tre inibitori della proliferazione cellulare, rende le cellule femminili suscettibili alla crescita tumorale allo stesso livello di quelle maschili. Al contrario, astrociti maschili di glioblastoma esprimono livelli più alti di proteine, quali Hmga2 and SHH, coinvolte nella progressione e nella disseminazione del tumore.
A livello epigenetico è stato osservato un incremento di metilazione che porta all’inattivazione del promotore della O6-Metilguanina-DNA metiltransferasi (MGMT), particolarmente rilevante a livello clinico: infatti il promotore del MGMT è inattivato nel 80% delle donne affette da glioblastoma e solo nel 27% degli uomini e tale ridotta funzione è associata a una migliore risposta alla chemioterapia e alla migliore prognosi osservata nelle donne.
Sono note differenze importanti nella risposta immunitaria, in generale più efficiente nelle donne. Dati recenti suggeriscono che le differenze osservate nella prevalenza delle malattie cerebrali, nelle caratteristiche cliniche e nella prognosi, siano legate a differenze a livello immunologico.
L’individuazione delle differenze sesso-specifiche non solo spiega le basi della patogenesi, ma in prospettiva rappresenta anche una fase fondamentale nell’individuazione di nuovi bersagli terapeutici per trattamenti realmente personalizzati, particolarmente importanti per patologie ancora prive di terapie veramente efficaci.
Bibliografia
Mayo Clinic. Glioblastoma (Inglese)
Fondazione Umberto Veronesi. Magazine. Glioblastoma: aumenta la sopravvivenza, soprattutto nelle donne
Istituto Superiore di Sanità, Ufficio stampa. Comunicato Stampa n°25/2017. Riprodotto in provetta glioblastoma, il più aggressivo tumore al cervello, per aprire la strada a efficaci cure personalizzate. Su “Neuro Oncology” lo studio condotto da team ricercatori Università Cattolica-Fondazione Policlinico Universitario A. Gemelli e Istituto Superiore di Sanità
Link approfondimento
Associazione Italiana per la Ricerca sul Cancro (AIRC). Tumore del cervello
Osservatorio Malattie Rare (OMaR). Glioblastoma
National Institutes of Health (NIH). National Cancer Institute. NCI Dictionary of Cancer Terms. Glioblastoma (Inglese)
Prossimo aggiornamento: 1 Aprile 2027




























