Introduzione
La miastenia gravis (MG) è una malattia rara causata da una risposta immunitaria anomala (autoimmune) che compromette la comunicazione fra i nervi e i muscoli, provocando affaticamento e debolezza muscolare (il termine miastenia, di origine greca, significa muscolo senza forza). Si manifesta in modo variabile e, generalmente, ha un andamento progressivo nel tempo (cronico).
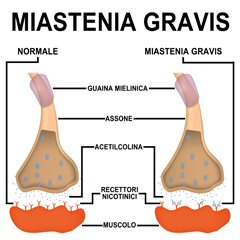
La MG è una malattia autoimmune, ciò significa che il sistema di difesa dell'organismo (sistema immunitario) aggredisce per errore alcune parti del corpo perché non le riconosce come proprie. Nella MG l'organismo produce anticorpi che impediscono a una molecola, l'acetilcolina, di trasmettere gli impulsi dal nervo al muscolo. La MG è quindi una malattia che colpisce la giunzione neuromuscolare; il muscolo della persona con MG è sano ma è indebolito, in quanto l'impulso per la contrazione muscolare non passa o è insufficiente.
In genere, la MG si manifesta con disturbi della vista, descritti soprattutto come sdoppiamento dell'immagine, e con l'abbassamento di una o entrambe le palpebre. Altri sintomi frequenti sono difficoltà di masticare e ingoiare. Alcuni pazienti sviluppano debolezza muscolare generalizzata. La debolezza muscolare è fluttuante, peggiora con l'attività e migliora con il riposo.
La MG colpisce entrambi i sessi; può comparire a qualsiasi età, dai bambini agli anziani, ma si manifesta più frequentemente tra 20 e 40 anni nelle femmine (forma a esordio precoce), e oltre i 50 anni nel sesso maschile (forma a esordio tardivo).
Non esiste ancora una cura risolutiva per la MG ma diverse terapie aiutano a tenere sotto controllo i disturbi (sintomi).
Sintomi
La miastenia gravis (MG) è caratterizzata da debolezza e affaticamento dei muscoli volontari, ovvero dei muscoli del corpo umano che si contraggono quando una persona lo vuole. La gravità della debolezza muscolare differisce da persona a persona, variando da deficit lievi e limitati a singoli gruppi muscolari a debolezza generalizzata. Il disturbo (sintomo) principale è l'esauribilità; la debolezza muscolare peggiora con l'attività e nelle ore serali e migliora dopo periodi di riposo. Il decorso della malattia è estremamente variabile; può essere caratterizzato da lunghi periodi durante i quali i disturbi diminuiscono o spariscono, oppure progredire rapidamente.
Il coinvolgimento dei muscoli oculari è molto frequente e si manifesta con l'abbassamento di una palpebra, o alternativamente delle palpebre dei due occhi (ptosi palpebrale), e con una visione doppia dell'immagine (diplopia). I disturbi oculomotori sono presenti nel 70-80% dei pazienti con MG. Nel 15% circa dei pazienti la malattia riguarda solo i muscoli oculari (miastenia oculare), ma nella maggioranza dei casi, generalmente entro i primi due anni dalla comparsa dei primi disturbi, la debolezza muscolare si estende ai muscoli di altre parti del corpo (miastenia generalizzata).
Il coinvolgimento dei muscoli del viso (muscoli mimici) provoca difficoltà nella chiusura degli occhi e una generale riduzione dell'espressività del volto. Quando sono coinvolti i muscoli masticatori, della faringe e della lingua si hanno difficoltà nella masticazione, nella deglutizione e nel parlare (la voce può diventare “nasale”). L'interessamento dei muscoli del collo, del tronco e degli arti può causare difficoltà nel mantenere la testa eretta, tenere le braccia sollevate, salire le scale o camminare a lungo. La compromissione dei muscoli del torace può causare difficoltà respiratorie, soprattutto in posizione sdraiata o dopo esercizio fisico.
In alcune persone possono verificarsi episodi improvvisi (acuti), definiti crisi miasteniche, caratterizzati da un rapido aggravamento della difficoltà a respirare e, talvolta, a deglutire, con debolezza agli arti. L'insufficienza respiratoria con necessità di ventilazione assistita è un evento grave che richiede l'immediato trasferimento del paziente in terapia intensiva. Tali crisi possono essere causate da infezioni, interventi chirurgici o farmaci controindicati nella miastenia.
Cause
Come per altre malattie autoimmuni, la causa della miastenia gravis (MG) non è conosciuta. Anche se la MG non è una malattia ereditaria si ritiene che predisposizione genetica e fattori ambientali ancora non ben definiti interagiscano nell'alterare il sistema di difesa dell'organismo (sistema immunitario) e provocare la produzione di autoanticorpi. Nella MG, gli autoanticorpi sono diretti contro due molecole che sono espresse sulla membrana delle cellule dei muscoli striati (detti anche muscoli volontari): il recettore dell'acetilcolina (AChR) e la tirosinchinasi muscolo-specifica (MuSK).
Gli anticorpi anti-AChR sono presenti nell’85% dei pazienti con MG generalizzata e nel 50% circa dei casi di miastenia oculare; sono particolarmente frequenti nella MG a esordio tardivo. Questi autoanticorpi si legano ai recettori dell’acetilcolina provocandone la distruzione; il numero di recettori sulla membrana della cellula muscolare risulta quindi diminuito. Di conseguenza, il neurotrasmettitore rilasciato dal nervo motore, l’acetilcolina, non è più in grado di esercitare la sua azione, ovvero regolare la contrazione dei muscoli. La MG con anticorpi anti-AChR si associa spesso ad alterazioni del timo, come ingrossamento (iperplasia) e timoma, un tumore delle cellule epiteliali timiche, quasi sempre di natura benigna. Il timo è una ghiandola situata tra i due polmoni e ha il compito di ‘istruire’ il sistema immunitario a non attaccare le cellule dell’organismo. L’ingrossamento del timo (iperplasia timica) è in genere associato alla forma a esordio giovanile, più frequente nelle donne. Il timoma è presente nel 15-20% dei pazienti, soprattutto fra i 40 e 60 anni di età. Si ritiene che nel timo si verifichino le alterazioni che inducono la produzione di autoanticorpi anti-AChR.
In una minoranza dei pazienti con MG (5-8%) sono prodotti anticorpi contro una molecola chiamata MuSK, che è importante per la distribuzione e quindi la funzione dei recettori dell’acetilcolina sulla membrana muscolare. Il blocco della funzione di MuSK da parte degli autoanticorpi provoca una grave alterazione della trasmissione neuromuscolare. A differenza della miastenia con anticorpi anti-AChR, nella miastenia con anticorpi anti-MuSK le forme oculari sono rare, sono colpiti maggiormente i muscoli facciali, oro-faringei e respiratori, i deficit degli arti sono generalmente lievi o assenti, e non sono presenti alterazioni significative del timo.
Più raramente, le persone con MG producono autoanticorpi contro altre due molecole presenti sulle cellule muscolari, chiamate LRP4 e agrina; questi autoanticorpi sono spesso presenti in associazione con gli anticorpi anti-AChR o anti-MuSK.
Diagnosi
I primi disturbi che possono indurre il sospetto di miastenia gravis (MG) sono i deficit di forza fluttuanti e l'affaticabilità muscolare. L'accertamento (diagnosi) si basa sulla dimostrazione di un disturbo della trasmissione neuromuscolare mediante l'elettromiografia e sulla rilevazione di autoanticorpi specifici. Un altro elemento a favore dell’accertamento di MG è la risposta immediata a un tipo di farmaci, chiamati anticolinesterasici, che favoriscono la trasmissione neuromuscolare.
Elettromiografia
È un esame strumentale che permette di valutare la risposta del muscolo alla stimolazione di un nervo motore, e quindi di rilevare il blocco della trasmissione neuromuscolare che nelle persone con MG è dovuto alla riduzione dei recettori dell’acetilcolina sul muscolo. L’esame consiste nell’inserire nei muscoli dei piccoli aghi collegati a degli elettrodi per misurare la trasmissione dell’impulso elettrico dal nervo al muscolo. L'elettromiografia a singola fibra permette di valutare l’attivazione di singole fibre muscolari innervate dalla stessa terminazione nervosa; questa indagine è utile per evidenziare un difetto della trasmissione neuromuscolare nei pazienti con disturbi lievi o non rilevabili.
Dosaggio degli anticorpi anti-AChR e anti-MuSK nel sangue
È un test molto specifico e un risultato positivo in un paziente che presenta sintomi compatibili con la MG conferma la diagnosi. Tuttavia, un risultato negativo del test non esclude la MG ed è consigliabile ripetere il dosaggio. La quantità di autoanticorpi non è indicativa della gravità della malattia ma può variare con il quadro clinico e la risposta alla terapia. La riduzione netta dei disturbi dopo somministrazione di farmaci è un altro elemento a favore della diagnosi di MG. I farmaci anticolinesterasici aumentano la disponibilità del neurotrasmettitore acetilcolina e quindi migliorano la trasmissione neuromuscolare, consentendo ai recettori residui sul muscolo di attivarsi ripetutamente. Attualmente, il test farmacologico utilizza la neostigmina per via intramuscolare; la risposta si manifesta in circa 15-20 minuti e dura per circa un’ora. Per questo test può anche essere usata la piridostigmina somministrata per via orale.
Indagini radiologiche
Una volta accertata la MG è indicata l'esecuzione di esami radiologici come la tomografia assiale computerizzata (TAC) o la risonanza magnetica nucleare (RM) del torace per verificare se il timo sia ingrossato o sia presente un tumore (timoma). Gli esami radiologici sono inoltre consigliati poiché il timoma può insorgere, anche se raramente, in pazienti con anticorpi diversi da quelli anti-AChR o in pazienti senza autoanticorpi rilevabili (miastenia sieronegativa). È opportuno effettuare anche il dosaggio degli ormoni tiroidei e degli anticorpi anti-tiroide, in quanto la MG è frequentemente associata con malattie della tiroide. Una TAC o RM cerebrale può anche essere eseguita per escludere che i disturbi possano essere causati da un problema al cervello.
Terapia
Le attuali terapie per la miastenia gravis (MG) possono ridurre i disturbi (sintomi) e migliorare la qualità di vita dei pazienti. La terapia della MG va adattata per quanto possibile al singolo paziente, tenendo conto di vari fattori, quali gravità dei disturbi, autoanticorpi responsabili della malattia, alterazioni del timo, età dell’individuo e concomitanza di altre patologie (comorbidità).
Farmaci
Comprendono farmaci sintomatici che hanno lo scopo di controllare i disturbi (sintomi) e farmaci immunosoppressori che agiscono sul sistema immunitario per ridurre le reazioni autoimmuni alla base della malattia.
Farmaci anticolinesterasici
La piridostigmina è il farmaco più utilizzato come primo trattamento della MG. Aumenta i livelli dell’acetilcolina in corrispondenza dei recettori neuromuscolari, migliorando la contrazione dei muscoli; può ridurre o eliminare i disturbi (sintomi) ma non agisce sulle cause della malattia. Poiché l’effetto del farmaco dura 3-4 ore è necessario assumerlo più volte al giorno. La piridostigmina può causare effetti indesiderati (effetti collaterali), quali crampi allo stomaco e ai muscoli, diarrea, aumento della salivazione, aumento delle secrezioni bronchiali, malessere generale, che generalmente scompaiono riducendo il dosaggio del farmaco. I farmaci anticolinesterasici non sono indicati per le persone con anticorpi anti-MuSK, nelle quali gli effetti collaterali sono particolarmente marcati.
Farmaci immunosoppressori
Nel caso in cui i farmaci anticolinesterasici non siano in grado di tenere sotto controllo i disturbi è necessario ricorrere ai farmaci immunosoppressori; questi farmaci riducono l'attività del sistema immunitario impedendo la produzione degli anticorpi e, di conseguenza, anche degli autoanticorpi anti-AChR e anti-MUSK che sono alla base della miastenia gravis.
Gli steroidi o cortisonici, in genere il prednisone, sono i farmaci immunosoppressori utilizzati per primi per la rapidità d’azione ed elevata efficacia; possono causare un peggioramento transitorio dei sintomi nelle prime settimane di cura. La somministrazione cronica di steroidi può causare effetti indesiderati (effetti collaterali), come aumento di peso, alterazioni dell'umore e aumento del rischio di infezioni. Se la terapia con gli steroidi non è sufficiente a ridurre i sintomi o deve essere usata ad alte dosi per un lungo periodo, è consigliato l’uso di farmaci immunosoppressori quali azatioprina, micofenolato mofetile, ciclosporina e ciclofosfamide. Questi farmaci permettono di ridurre il dosaggio degli steroidi e possono sostituire il prednisone nella terapia a lungo termine; possono indurre seri effetti indesiderati (effetti collaterali) come aumento del rischio d’infezioni, e problemi al fegato o ai reni, per prevenire i quali sono necessari appropriati controlli periodici.
Farmaci biologici
In caso di mancata risposta ai farmaci immunosoppressori o necessità di alti dosaggi di steroidi e altri immunosoppressori con effetti collaterali gravi, è stata di recente presa in considerazione la somministrazione dei cosiddetti farmaci biologici. Numerosi studi hanno evidenziato un miglioramento dei sintomi e della qualità della vita delle persone con MG trattate con rituximab, un anticorpo monoclonale che provoca la rapida distruzione dei linfociti B, le cellule che producono anticorpi. L’utilizzo di questo farmaco richiede un’accurata valutazione sia prima che durante il trattamento per il rischio di complicanze infettive ed ematologiche.
Plasmaferesi
È una procedura che permette di rimuovere dalla parte di sangue priva di cellule (plasma) molecole dannose, come gli autoanticorpi. La plasmaferesi riduce rapidamente la concentrazione degli autoanticorpi responsabili della MG e viene in genere utilizzata come terapia di emergenza nelle fasi di peggioramento della malattia.
Immunoglobuline umane ad alto dosaggio
Un'alternativa alla plasmaferesi è la somministrazione endovenosa di immunoglobuline ad alto dosaggio provenienti dal sangue di un donatore. Le immunoglobuline, efficaci anche in altre malattie immunitarie, agiscono sul sistema immunitario inibendo la produzione e gli effetti degli autoanticorpi responsabili della MG. La plasmaferesi e le immunoglobuline ad alto dosaggio non sostituiscono la terapia immunosoppressiva farmacologica; grazie alla rapida efficacia, queste terapie sono estremamente utili nelle forme più gravi di MG e, in associazione al prednisone ad alte dosi, nel trattamento delle crisi respiratorie.
Intervento chirurgico (asportazione del timo)
L’asportazione del timo (timectomia) viene effettuata soprattutto nelle persone con MG associata ad anticorpi anti-AChR. L'intervento chirurgico è indicato nei pazienti con timoma; nei casi in cui non si riscontri un timoma, l'opportunità di rimuovere il timo deve essere valutata in base alle caratteristiche di ogni paziente. Soprattutto nei casi con esordio giovanile, la timectomia costituisce un'opzione terapeutica utile per ridurre il dosaggio di farmaci immunosoppressori e migliorare i sintomi. In genere, è un intervento che viene programmato dopo aver raggiunto un buon controllo dei sintomi con la terapia farmacologica.
È noto che diversi farmaci interferiscono con la trasmissione neuromuscolare e devono essere evitati nelle persone con MG, o utilizzati con prudenza sotto stretto controllo medico, in quanto possono peggiorare i sintomi della malattia. Tra i farmaci controindicati sono presenti alcune classi di antibiotici, antimalarici, antireumatici, antiaritmici e ansiolitici.
In Italia, la MG è inserita nell'elenco delle malattie rare esenti dal costo del ticket (Decreto del Presidente del Consiglio dei Ministri del 12 gennaio 2017, Allegato 7) con il codice RFG101 all'interno del gruppo Sindromi miasteniche congenite e disimmuni.
Per altre informazioni sulla MG (centri di diagnosi e cura, associazioni di pazienti) è possibile rivolgersi al Telefono Verde Malattie Rare (TVMR) 800.89.69.49. Il numero è attivo dal lunedì al venerdì dalle 9:00 alle 13:00.
A livello europeo la MG è studiata all’interno della Rete Europea di Riferimento per le malattie neuromuscolari rare [European Reference Network for Rare Neuromuscular Diseases (EURO-NMD). Scopo del Network è armonizzare e indicare le migliori pratiche per l'accertamento (diagnosi) e la cura della malattia, migliorare l'equità delle prestazioni di assistenza negli Stati membri, ridurre i tempi necessari ad accertare la malattia, offrire formazione e istruzione specialistica, realizzare servizi di sanità elettronica, sviluppare linee guida per l'assistenza, promuovere la ricerca traslazionale e clinica e condividere dati di alta qualità.
Bibliografia
Narayanaswami P, Sanders DB, Wolfe G, Benatar M, Cea G, Evoli A, Gilhus NE, Illa I, Kuntz NL, Massey J, Melms A, Murai H, Nicolle M, Palace J, Richman D, Verschuuren J. International Consensus Guidance for Management of Myasthenia Gravis: 2020 Update. Neurology. 2021 Jan 19; 96(3): 114-122
Link approfondimento
Associazione Italiana Miastenia e Malattie Immunodegenerative (AIM) – Amici del Besta Onlus
Associazione Italiana MIAstenia onlus
Ministero della Salute. Centri di diagnosi e cura. Centri specializzati per miastenia gravis
Prossimo aggiornamento: 29 Dicembre 2023




























